
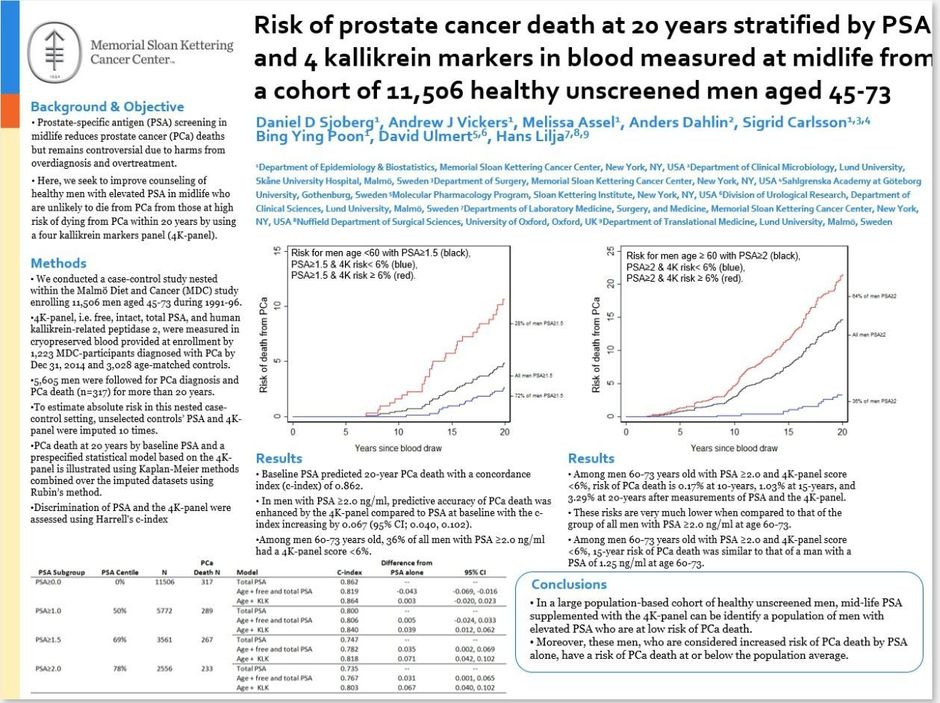
Een groep Amerikaanse en Europese vorsers (1) heeft een oude cohorte, die werd gevormd in de jaren negentig, geanalyseerd en gedurende 20 jaar gevolgd (n = 5.306). In die cohorte zijn 317 patiënten gestorven aan prostaatkanker. De researchers hebben onder meer het PSA-gehalte en de kallikreïnespiegel gemeten. Ter herinnering, kallikreïne-3 is in feite PSA.
Patiënten met laag risico opsporen
De internationale groep heeft onder meer het aan kallikreïne gerelateerde peptidase 2 bepaald. Op die manier konden ze veel preciezer voorspellen welke patiënten dreigden te sterven. Bij patiënten van 60-73 jaar met een PSA-gehalte van 2 of hoger en een samengestelde score met o.a. kallikreïne lager dan 6% bedroeg de sterfte aan prostaatkanker 0,17% 10 jaar, 1% 15 jaar en 3,29% 20 jaar na de initiële meting. Dat risico was heel wat lager dan het risico dat werd berekend op grond van het PSA-gehalte alleen. Toevoeging van kallikreïne vormt dus een discriminerende factor bij patiënten met een prostaatkanker met een laag of een hoog risico, waardoor je overbehandeling kan tegengaan.
6-14% van de mannen vertoont gemuteerde genen. Die mutaties zijn dan ook één van de belangrijkste genetische oorzaken van agressieve prostaatkanker. Die mannen lopen driemaal meer kans op een agressieve kanker
Hoog risico opsporen
Dat strookt met het genetische onderzoek van Alexandre Zlotta en zijn Canadese collega's (2). We kennen nog 14 andere proteasegenen die dicht bij de kallikreïneregio op chromosoom 19 liggen. Recent onderzoek heeft uitgewezen dat die regio tal van mutaties kan vertonen. Vaak betreft het een verandering van één enkele nucleotide, een SNP (spreek uit als "snip") voor Single Nucleotide Polymorphism. Zo'n SNP kan echter correleren met een agressieve prostaatkanker. De Canadese onderzoekers hebben de gegevens doorgenomen van 1.858 patiënten met een agressieve prostaatkanker (Gleasonscore > 8) in Europa, de VS en Canada.
Er werden verschillende SNP's geïdentificeerd in de KLK6-regio met hetzelfde haplotype bij patiënten met een agressieve prostaatkanker, zowel bij de patiënten in de studie als in de valideringscohorte. In de valideringscohorte hebben de onderzoekers twee nieuwe haplotypes op dezelfde locus ontdekt die ook correleren met een ernstigere kanker.
"6-14% van de mannen vertoont gemuteerde genen. Die mutaties zijn dan ook één van de belangrijkste genetische oorzaken van agressieve prostaatkanker. Die mannen lopen driemaal meer kans op een agressieve kanker", legde de Canadees uit. Dat vertegenwoordigt dus een groot deel van de 10-15% agressieve prostaatkankers. "Zelfs als je alleen kijkt naar de 6% mannen met die mutatie, dan nog gaat het om 17 miljoen Noord-Amerikanen en 22 miljoen Europeanen", preciseerde de Canadese specialist.
De behandeling aanpassen
Die kiemcelmutaties predisponeren ook tot een recidief, ongeacht de gebruikelijke klinische en moleculaire factoren. "We hebben inderdaad ontdekt dat de frequentie van recidief 3-maal hoger was bij mannen met die mutaties die werden behandeld met chirurgie of radiotherapie, dan in de rest van de bevolking. De onderzoekers zouden een test willen ontwikkelen die voldoende praktisch is voor routinegebruik. Het is immers belangrijk een prostaatkanker met een laag risico te onderscheiden van andere vormen van prostaatkanker, maar het is minstens even belangrijk om zo snel mogelijk de patiënten op te sporen die het hoogste risico lopen op een agressieve kanker. Dan zou je die patiënten snel een geschikte behandeling kunnen geven. Als die genetische tests zijn gevalideerd, zou het zeker goed zijn mochten we ze in de routinepraktijk kunnen gebruiken.
- Sjoberg DD et al. Risk of prostate-cancer death at 20 years stratified by midlife PSA and a panel of four kallikrein markers from a representative cohort of 11,506 healthy unscreened men aged 45-74. EAU 2017 - Abstract#240
- Briollais L et al. Germline mutations in the Kallikrein 6 region and predisposition for aggressive prostate cancer. EAU 2017 - Abstract #356

