...
Nivolumab biedt potentieel bij gevorderd HCC
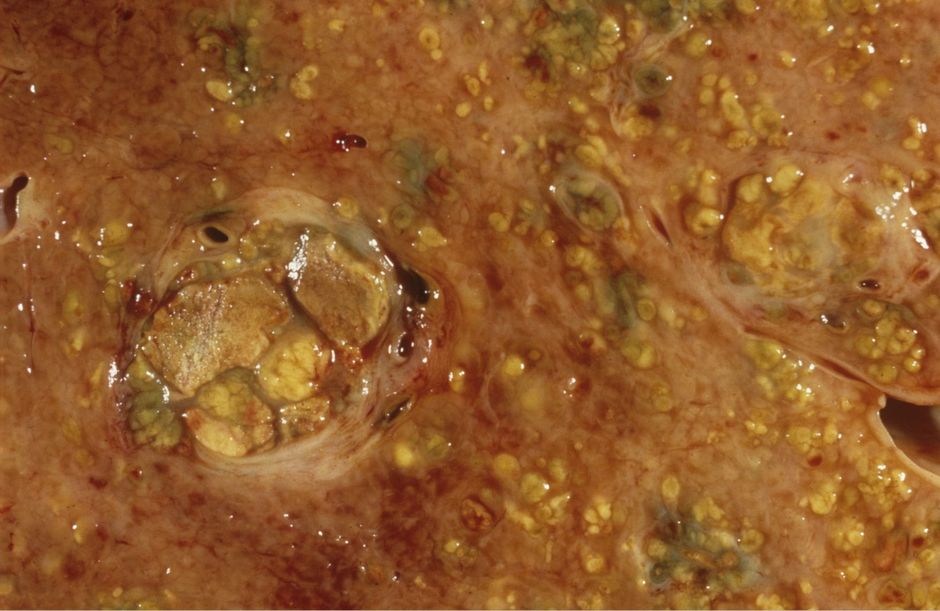
Voor patiënten met gevorderd hepatocellulair carcinoom (HCC) beschikken we momenteel alleen over sorafenib als systemische medicatie. Hoe doet nivolumab, een PD-1 inhibitor, het in deze indicatie en is deze checkpoint inhibitor wel veilig?
Verder lezen?
Registreer u om toegang te krijgen tot de inhoud van deze website.* Lees bovendien elke maand 4 gratis artikelen
Ik registreer mij Ik ben al geregistreerd* Artsenkrant, Belgian Oncology & Hematology News, ak update Specialist zijn medische vakbladen. De Belgische wetgeving zegt dat alleen artsen en zorgverleners met Rizivnummer deze mogen raadplegen. Dat geldt ook voor deze sites.
ak update Specialist-clubleden hebben onbeperkt toegang tot alle artikelen
Ik wil lid worden Ik ben al lidVerder lezen?
Registreer u om toegang te krijgen tot de inhoud van deze website.* Lees bovendien elke maand 4 gratis artikelen
Ik registreer mij Ik ben al geregistreerd* Artsenkrant, Belgian Oncology & Hematology News, ak update Specialist zijn medische vakbladen. De Belgische wetgeving zegt dat alleen artsen en zorgverleners met Rizivnummer deze mogen raadplegen. Dat geldt ook voor deze sites.
ak update Specialist-clubleden hebben onbeperkt toegang tot alle artikelen
Ik wil lid worden Ik ben al lid